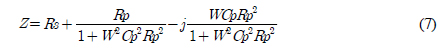3. 실험결과 및 고찰
Fig. 3은 각각의 pH용액에서 측정된 부식전위의 변화를 보여주고 있다. pH가 10.5 및 9.6의 용액에서는 침지시간의 증가와 함께 부식전위는 상승하였으며 pH가 7.2와 8.5의 경우에는 침지시간의 변화와 함께 부식전위는 낮은 방향으로 이행하는 경향을 알 수 있다. 전술한 바와 같이 최근의 수돗물은 고도정수 처리과정을 위하여 과량의 염소를 투입함에 따라 전술한 이론적 고찰에서 언급한 바와 같이 차아염소산이온과 염소이온이 수돗물에 많이 존재하게 된다. 따라서 pH가 낮은 용액의 경우 시험용액에 존재하는 차아염소산이온과 염소이온에 의한 산화피막의 파괴에 의해서 혹은 염소이온 등의 음이온이 시험편 표면에 흡착하여 부식전위는 낮은 방향으로 이행하는 것으로 생각된다(
Jeon, 1985). 그리고 전기분해에 의해서 pH가 높은 알카리수를 음극실에서 생성할 경우 음극실에 있는 음이온 즉 차아염소산이온과 염소이온이 중성실을 통하여 양극실로 이동함으로써 음극실에서 생성된 알카리수에는 음이온이 적게 함유되어 염소이온과 같은 음이온에 의한 표면의 산화피막파괴가 억제되고 또한 알카리수에 많이 함유되어 있는 수산화이온에 의한 산화막의 생성에 의해서 부식전위는 침지시간의 변화와 함께 높은 방향으로 이행하는 것으로 생각된다.
Fig. 3
Variation of corrosion potentials with immersion time in each solution as a function of pH
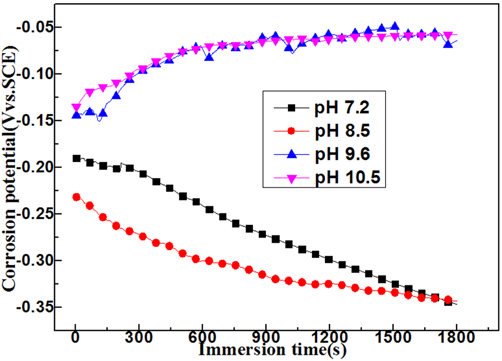
Fig. 4는 교류 임피던스 측정에 의한 실수부와 허수부의 임피던스의 변화선도(Cole-cole plots)를 나타내고 있다. 그런데 용액 중에 침지되어 있는 시험편의 경우 용액과 시험편의 계면에는 임피던스와 전기 2중층이 존재하며 시험편의 표면 상태에 따라서 임피던스와 전기 2중층이 직렬과 병렬회로 혹은 더욱 복잡한 병렬회로 및 확산 등의 등가회로 등으로 구성되는 것으로 보고되고 있다(
Allen and Harry, 1980a;
Allen and Harry, 1980b;
Grahame, 1952). 그리고 이러한 등가회로의 추측은 임의의 등가회로를 가정하고 임피던스와 전기 2중층의 임의의 적당한 값을 대입하여 시뮬레이션에 의한 실수부와 허수부의 임피던스의 값에 따른 다양한 형태의 변화선도(Cole-cole plots)를 구한 후 실제의 실험을 통하여 주파수에 따른 실수부와 허수부 값에 따른 선도(Cole-cole plots)를 측정하고 이 선도와 시뮬레이션에 의해서 구한 가상의 선도와 동일한 형태의 선도가 나타 날 경우 임의의 등가회로를 실제의 용액과 계면에 존재하는 등가회로로 추측할 수 있게 된다. 본 실험에서 임피던스 측정 장치에 의해서 측정한 실수부와 허수부의 측정결과는
Fig. 4에서 알 수 있듯이 정성적으로 반원형의 모습을 보여 주고 있다. 그러나 확실한 등가회로를 추측하기 위해서는 주파수가 제로에 근접하는 값까지 측정하는 것이 바람직하나 이 경우 무한대의 시간이 소요되는 실험상의 어려움 때문에 본 실험에서는 0.01Hz까지 측정한 결과를
Fig. 4에서 보여주고 있다. 일반적으로 나 강판(Bare steel plate)의 시험편이 해수용액에 침지되어 있을 경우 실수부와 허수부의 교류 임피던스의 측정 결과는 반원형을 나타내는 경우가 많다. 그런데 본 실험의 경우 해수가 아닌 수돗물의 경우 각각의 pH를 달리한 경우에도 해수에서 측정한 결과와 유사한 결과를 얻을 수 있었다. 따라서 이 경우 등가회로는 다음의
Fig. 5의 병렬 등가회로를 예상하게 된다.
Fig. 4
Comparison of Cole-cole plots with various pH solutions
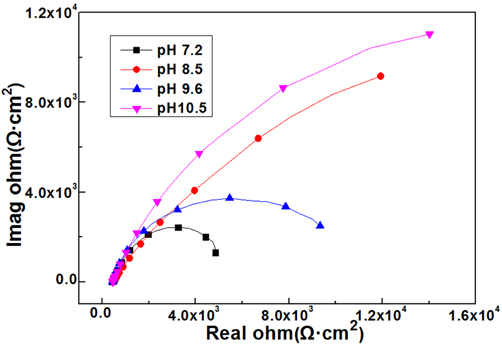
Fig. 5
Eequivalent circuit diagram by parallel circuit of polarization resistance and electric double layer capacity
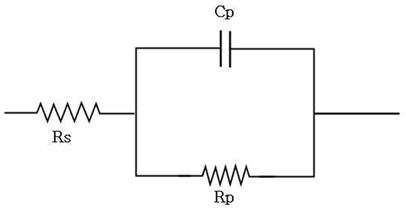
Rs : Solution resistance, Rp : Polarization resistance, Cp : Electric double layer capacity
그리고 이 등가회로에 의한 임피던스를 구하는 이론식은 다음과 같다. 즉 임피던스 Z는 다음 식 (7)로 나타내어진다.
상기 식 (7)에서 주파수와 전기2중층 용량 및 분극저항을 적당한 값으로 시뮬레이션 하면
Fig. 6의 반원형으로 나타나게 된다. 그리고 상기 식 (7)에서 주파수(
W=
2ℼf)가 무한대로 되면 실수부와 허수부가 제로 값이 되며
Fig. 6에서도 알 수 있듯이 주파수가 무한대로 클 경우 임피던스
Z는
Rs로 되며 즉 용액저항만을 나타내게 된다. 그리고 주파수가 제로에 가까워지면 상기 식 (7)에서 알 수 있듯이 허수부는 제로가 되며 실수부의 분극저항만 남게 된다. 따라서 임피던스
Z는
Rs +
Rp가 된다. 그러나 실제의 실험에서 임피던스를 측정할 경우 시험편 혹은 시험용액에 대한 상대평가이므로 용액저항(
Rs)의 값은 적으므로 크게 문제 되지 않으며 주파수가 제로인 경우의 임피던스 즉 용액저항(
Rs)과 분극저항(
Rp)을 합한 임피던스(
Z)에 대해서 상대평가를 주로 많이 하게 된다. 따라서
Fig. 5의 등가회로를 예상하고 시뮬레이션 할 경우
Fig. 6의 전형적인 반원형이 나타나게 된다. 본 실험의 경우에도 실제로 측정한 결과는 즉
Fig. 4에서 알 수 있듯이 정성적으로
Fig. 6과 유사한 반원형의 모습을 보여 주고 있으므로 결국 본 실험의 시험편과 용액계면사이에는 전기 2중층과 분극저항이 병렬회로 상태로 존재하고 있음을 추측 할 수 있다.
Fig. 7은 각각의 pH용액에서 측정한 주파수 변화에 따른 임피던스 값의 변화를 보여 주고 있다. 10
1에서 10
4 Hz까지의 임피던스 값은 pH에 관계없이 거의 같은 일정한 값을 보여주고 있음을 알 수 있다. 그리고
Fig. 6에서 주파수가 무한대로 될 경우의 임피던스는 용액저항(
Rs)을 나타냄으로
Fig. 7에서 비록 10
4 Hz가 무한대의 주파수는 아니지만 용액저항의 근사 값으로 볼 수 있으며 또한 용액의 종류에 관계없이 거의 같은 값을 나타내고 있음을 알 수 있다. 그리고
Fig. 6에서 알 수 있듯이 주파수가 제로 값에 근접할 경우의 임피던스 값은 용액저항과 분극저항을 포함한 임피던스(
Z =
Rs +
Rp)이므로 10
-2 Hz에서의 임피던스 값은 비록 주파수가 제로 값은 아니지만 제로에 근접한다고 할 수 있으므로
Fig. 7의 10
-2 Hz에서 측정된 임피던스 값을 pH의 종류에 따른 시험편 계면에서의 분극저항의 상대적인 대소 값으로 평가 할 수 있다고 생각된다. 따라서
Fig. 7에서 알 수 있듯이 pH가 7.2인 용액에서 분극저항이 가장 적으며 pH가 10.5인 용액에서 분극저항이 가장 높은 값을 나타내고 있음을 알 수 있다. pH가 낮은 7.2의 용액은 수돗물이므로 전술한 바와 같이 차아염소산 이온과 염소이온이 많이 함유되어 있어 시험편표면의 피막을 파괴하여 임피던스가 가장 낮은 값을 나타내는 것으로 생각되며 그리고 전기분해에 의해서 pH가 높은 알카리수를 음극실에서 생성할 경우 음극실에 있는 음이온 즉 차아염소산이온과 염소이온이 중성실을 통하여 양극실로 이동하여 음극실에서 생성된 알카리수에는 음이온이 적게 함유되어 염소이온과 같은 음이온에 의한 표면의 산화피막 파괴가 억제되고 또한 알카리수에 많이 함유되어 있는 수산화이온에 의한 산화막의 생성에 의해서 분극저항이 가장 높은 값을 나타내는 것으로 생각된다.
Fig. 6
Schematic diagram of AC impedance cole-cole plot
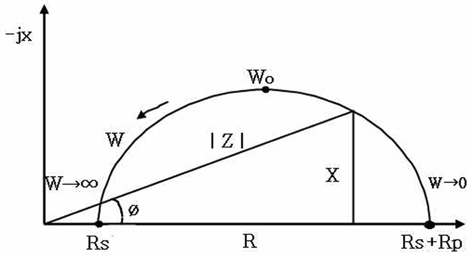
Fig. 7
Variation of impedance with frequency in various pH solutions
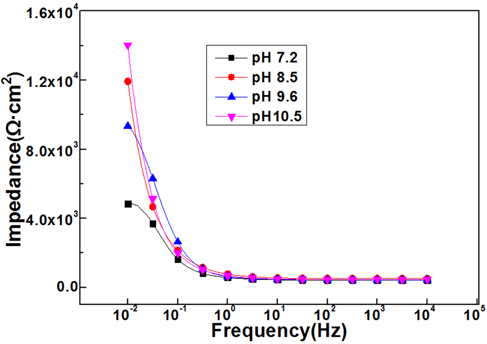
Fig. 8은 각각의 pH용액에서 측정한 첫 번째 사이클릭선도 변화를 보여주고 있다.
Fig. 8에서 알 수 있듯이 pH 7.2와 8.5용액의 사이클릭선도 형상은 공급전류밀도가 제로(0)인 점을 중심으로 양극전류밀도(플러스 값)영역에서는 오른쪽 방향으로 그리고 음극전류밀도(마이너스 값) 영역에서는 왼쪽방향으로 기울고 있음을 알 수 있다. 그러나 pH 9.6 및 10.5의 용액에서는 음극전류밀도 영역에서는 pH 7.2와 8.5용액과 거의 유사한 형태로 기울고 있으나 공극전류밀도 값이 약 제로 값에 근접하는 양극 전류밀도 영역에서는 사이클릭선도는 수직의 형태를 나타내고 있다. 이것은 시험편의 계면에서 양극분극이 일어날 경우 알카리수의 경우에는 즉 pH 9.6과 10.5의 용액에서는 염소산이온과 염소이온 등의 음이온이 적어 계면에서 음이온에 의한 산화피막의 파괴가 억제되어 부동태피막과 유사한 산화피막의 형성에 의한 저항분극의 증가로 사이클릭선도가 수직의 형태를 나타내는 것으로 생각된다. 그리고 pH 7.2와 8.5용액의 경우에는 용액중에 잔존하고 있는 음이온이 양극분극 시에 시험편 계면에서 산화피막을 파괴하여 즉 활성화되어 사이클릭선도는 오른쪽으로 기우는 것으로 생각 된다. 그리고 음극전류밀도 영역에서는 음이온의 영향을 받지 않는 환원반응 즉 용존산소 등에 의한 환원반응에 의한 선도변화이므로 pH 값의 변화에 따른 용액에 상관없이 비슷한 형태의 선도변화를 나타내는 것으로 생각된다.
Fig. 9는 10번째의 사이클릭선도 변화를 보여 주고 있다.
Fig. 8의 첫 번째 사이클릭선도 변화와 거의 유사한 양상을 나타내고 있음을 알 수 있다.
Fig. 8에서 토론한 바와 같이
Fig. 9에서도 양극분극 영역에서 알카리수의 경우 즉 pH 9.6과 10.5의 용액에서는 염소이온 등의 음이온에 의한 피막의 파괴영향이 적어 치밀한 산화피막의 형성에 의해 수직형태의 선도변화를 보여주고 있으며 반면에 수돗물과 같은 중성의 용액 즉 pH 7.2 및 8.5의 용액에서는 음이온이 많이 함유되어 있어 이들 음이온에 의해 산화피막이 파괴되어 오른쪽으로 기울어진 활성태의 선도 변화를 보여주는 결과를 재확인 할 수 있었다.
Fig. 8
Variation of 1st cyclic voltammogram curves with various pH solutions
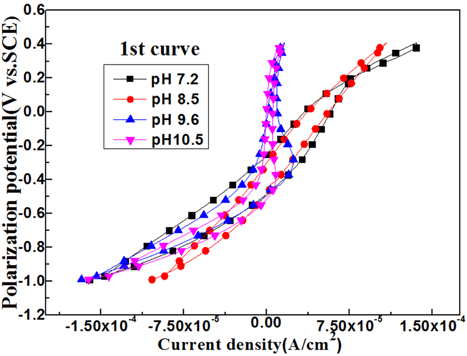
Fig. 9
Variation of 10th cyclic voltammogram curves with various pH solutions
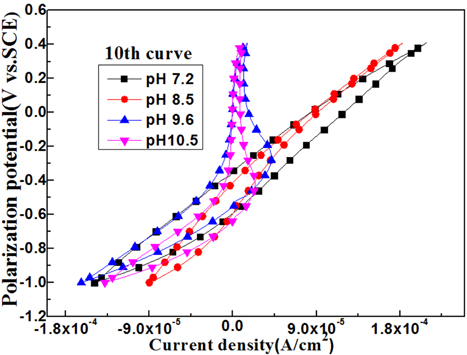
Fig. 10은 시험편을 각각의 pH 용액에 침지한 후에 유동과 비유동 상태로 하여 3일이 경과한 후의 부식된 표면상태를 보여주고 있다. 유동과 비유동에 관계없이 pH 10.5의 알카리수가 가장 부식이 적고 pH 7.2의 수돗물이 가장 부식이 큰 경향을 알 수 있다. 그리고 유동의 경우가 비유동에 비해서 외관상 붉은 녹이 뚜렷하게 많이 나타나는 경향도 알 수 있었다. 알카리수는 전술한 바와 같이 수돗물에 비하여 음이온의 함량이 적어 음이온에 의한 산화피막의 파괴에 따른 양극반응이 억제되고 또한 수산화이온(OH
-)의 함량이 많아 음극의 환원반응 즉 용존산소의 환원반응(O
2 + 2H
2O + 4e → 4OH
-)도 억제되어 부식속도의 감소에 의해 녹의 형성이 적은 것으로 생각된다. 그리고 수돗물은 알카리수와는 반대로 많은 양의 음이온과 적은 양의 수산화이온(OH
-)에 의해서 부식속도는 알카리수에 비해서 크고 결과적으로 붉은 녹의 형성도 심한 경향을 나타내는 것으로 생각된다.
Fig. 10
Comparison of corroded surfaces after 3 days immerged in various pH solutions(Arrows indicate flow direction)
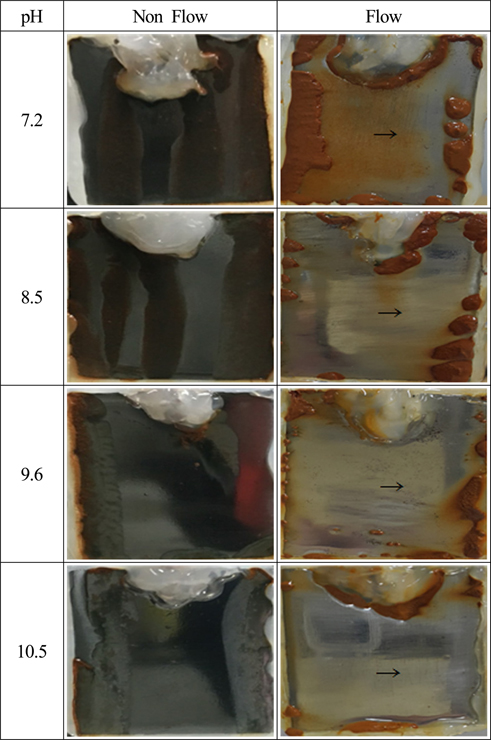
Fig. 11은 유동과 비 유동상태에서 침지 10일 후의 부식된 시험편의 표면 상태를 보여 주고 있다. 침지 3일 후에 비해서 유동과 비유동에 관계없이 전체적으로 붉은 녹의 생성이 뚜렷하고 그 양도 훨씬 많은 경향을 나타내었다. 그리고 비 유동의 경우가 유동에 비해서 시험편 표면에 덮혀 있는 붉은 녹의 크기가 유동에 비해서 훨씬 큰 경향을 나타내었다. 일반적으로 시험편에서의 녹의 발생은 시험편 표면에 무수히 존재하는 양극과 음극의 전위차에 의해서 발생하게 되므로 부식발생 초기에는 미세한 크기의 양극에서 붉은 반점의 녹이 형성되고 시간의 경과와 함께 점진적으로 붉은 녹은 시험편 전체로 확대되어 어느 일정기간이 지나면 시험편 전체가 붉은 녹으로 덮히게 된다. 그러나 전해질 용액이 유동할 경우 표면의 산화피막이 유실되어
Fig. 11에서 보여 주듯이 시험편 표면에서의 녹의 형성 양상이 비유동과 유동에서 상당히 차이를 나타내고 있음을 알 수 있다. 그리고
Fig. 11에서 붉은 녹으로 덮혀 있는 부위를 A, 외관상 붉은 녹이 없는 흰 바탕의 부위를 B로 표시하였다.
Fig. 12는
Fig. 11의 비 유동 상태에서 붉은 녹으로 덮혀 있는 A 부위의 녹을 제거하고 아세톤으로 세척한 후에 관찰한 표면상태를 보여 주고 있다. pH 값에 관계없이 모든 용액에서의 표면은 거의 같은 평활한 양상을 보여주고 있음을 알 수 있다. 결과적으로 붉은 녹의 산화물로 덮혀 있는 A 부위의 하부 바탕의 표면은 전면부식이 발생하고 있음을 알 수 있다. 이것은 붉은 산화물로 덮혀 있을 경우 용액에 있는 음이온이 붉은 녹물의 수산화 제2철(Fe(OH)
3)이 전리하여 생성된 3가 이온의 철과 반응하여 염화 제2철(FeCl
3)을 형성하여 소비되며 또한 녹의 생성물이 염소이온과 같은 음이온이 녹의 내부표면까지 침투하는 것을 막는 장벽 역활을 하여 내부 표면은 염소이온에 의한 국부부식이 발생하지 않고 전면부식이 발생하는 것으로 생각된다.
Fig. 11
Comparison of corroded surfaces(A,B) with flow and non flow after 10 days immerged in various pH solutions
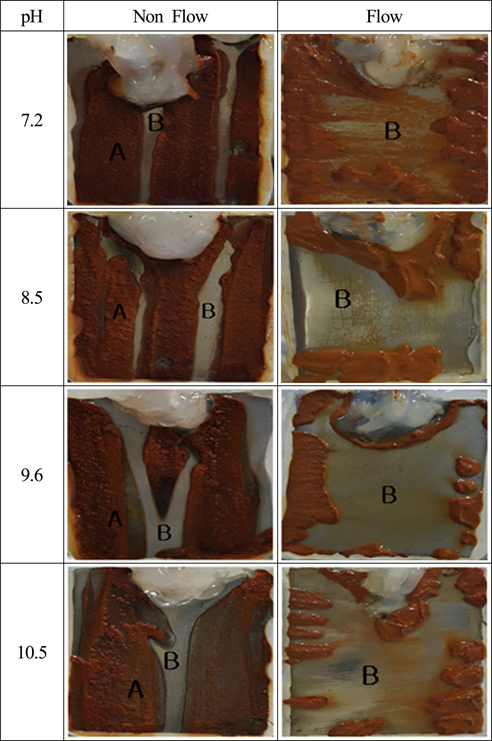
Fig. 12
Comparison of base surfaces removed rust oxide from A area after 10 days immerged in various pH solutions in case of non flow condition

Fig. 13은 비유동 상태에서
Fig. 11의 외관상 붉은 녹이 없는 흰 바탕의 B 부위를 아세톤으로 세척한 후에 관찰한 하부의 표면 상태를 보여 주고 있다.
Fig. 11에서 알 수 있듯이 흰 바탕의 B 부위는 녹의 산화물로 덮혀 있지 않는 다시 말해서 육안으로 보아 전혀 부식되지 않고 있는 것으로 착각할 수 있었으나 실제의 현미경 관찰에서는
Fig. 13에서 보여 주듯이 pH 10.5의 알카리수의 경우에는 표면이 전체적으로 평활한 형태를 보여주고 있으나 pH 7.2의 수돗물과 pH 8.5 및 9.6의 용액의 경우에는 표면에 공식과 같은 반점형태의 국부부식이 발생하고 있음을 알 수 있다. 결국 붉은 녹의 산화물로 덮혀 있지 않는 B 부위의 경우에는 용액의 염소이온이 시험편 표면에 쉽게 도달하여 먼저 염화 제1철(FeCl
2: : Fe
2+ + 2Cl
- → FeCl
2)을 형성하고 이들 염화 제1철은 물과의 반응 즉 가수분해 반응(FeCl
2 + 2H
2O → Fe(OH)
2 + 2HCl)에 의해 수산화 제2철(Fe(OH)
2)과 염산(HCl)을 생성 하여 시험편 표면의 오목부위의 pH를 저하시켜 국부부식을 발생시키는 것으로 생각된다. 다만 pH 10.5의 알카리수의 경우에는 알카리수의 생성과정 중 염소이온은
Fig. 2에서 알수 있듯이 중성실과 양극실로 이동하여 음극실의 알카리수에는 염소이온의 함량이 적어 전술한 염화 제 1철의 형성과 가수분해 반응이 억제되어 시험편 표면에서 국부부식이 발생하지 않는 것으로 생각된다.
Fig. 13
Comparison of base surfaces of B area after 10 days immerged in various pH solutions with non flow condition

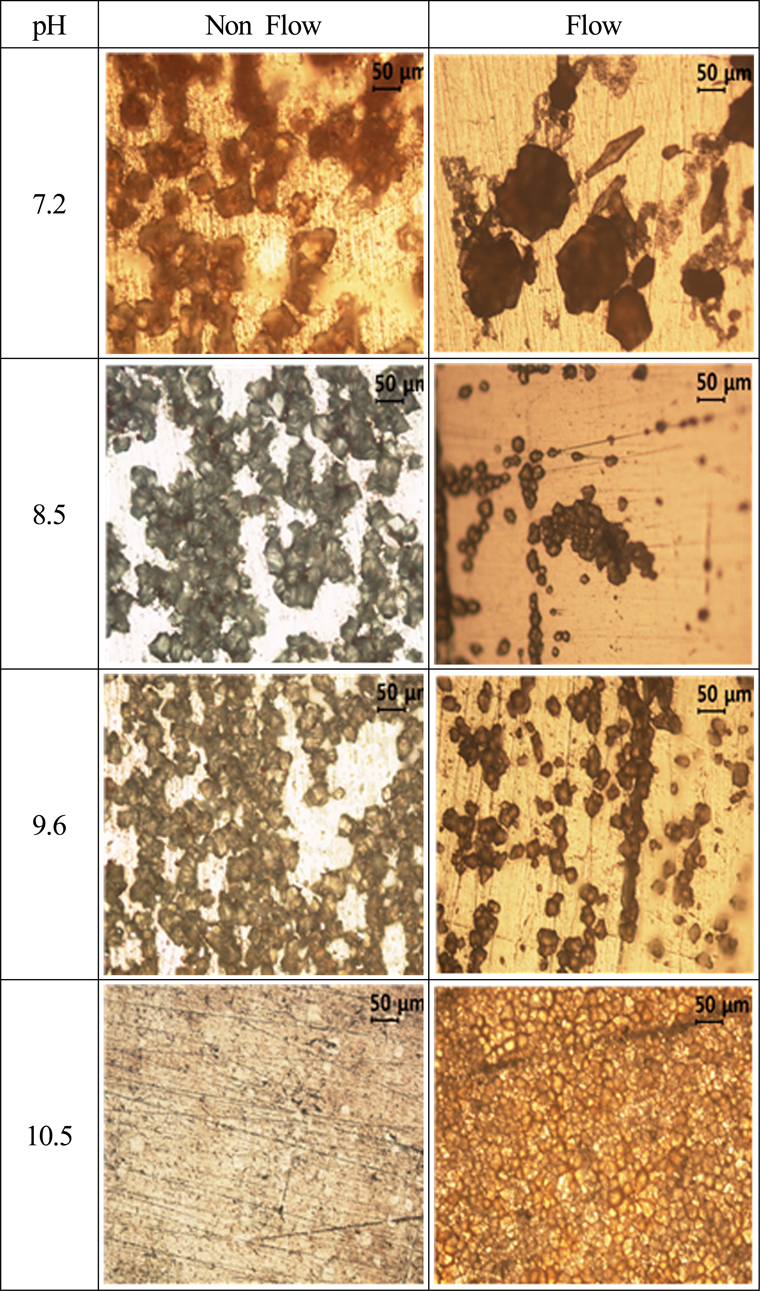
Fig. 14는
Fig. 11에서 표시한 비유동의 경우 흰 바탕의 B부위와 유동의 경우 흰 바탕의 B 부위에 대한 현미경 관찰 결과를 보여주고 있다. pH 10.5의 알카리수의 경우에는 비유동과 유동에 관계없이 표면에는 국부부식은 발생하지 않고 전면부식의 형태를 나타 내었으나 그 외의 다른 용액에서는 국부부식의 형태가 발견되었음을 알 수 있다. 그리고 특이한 점은 pH 7.2의 수돗물의 경우 유동의 경우가 비유동에 비해서 국부부식의 반점이 큰 경향을 알 수 있었다. 용액의 유동은 염소이온과 용존산소의 시험편 표면의 접근을 더욱 용이하게 하여 국부부식을 가속화시키는 것으로 생각된다.
Fig. 14
Comparison of corroded surfaces(B) after 10 days immerged in various pH solutions in case of non flow and flow condition
4. 결 론
지금까지 수돗물을 전기화학적으로 전기분해하여 알카리수를 생성시키고 생성된 알카리수와 기존의 수돗물을 혼합하여 4종류의 pH가 다른 시험용액을 만든 후 이들 용액의 부식특성을 SS 400강에 대하여 전기화학적으로 비교 관찰 하였다. 비교 관찰한 결과 다음과 같은 결론을 얻을 수 있었다.
(1) 수돗물(pH:7.2)을 전기분해하여 생성된 알카리수(pH:10.5)에 침지된 시험편의 부식전위는 상승하였고 기존의 수돗물에서는 하강하는 경향을 보였다.
(2) 알카리수(pH:10.5)에서 측정된 시험편 표면의 임피던스 값은 수돗물(pH:7.2)에 비하여 높은 값을 나타내었다.
(3) 사이클릭선도에서 알카리수(pH:10.5)는 양극분극시에 부동태 형태를 나타내었으나 수돗물(pH:7.2)의 경우에는 활성태 양상을 나타내었다.
(4) 수돗물(pH:7.2)에 침지된 시험편 표면에서는 국부부식이 발생되었으나 알카리수(pH:10.5)에서는 전면부식이 발생되었다.
(5) 결과적으로 수돗물(pH:7.2)을 전기분해하여 생성된 알카리수(pH:10.5)는 염소이온과 같은 음이온이 제거되고 수산화이온이 많이 함유되어 있어 수돗물에 비하여 우수한 내식성을 나타내는 것을 알 수 있었다.
(6) 본 연구의 결과는 각종 선박의 엔진과 열교환기 및 해양 플랜트 강구조물의 내식성 향상을 위한 유익한 참고자료가 되리라 기대된다.